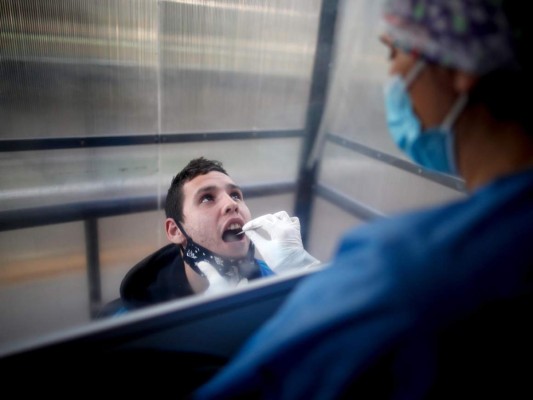
Esta prueba, que fue autorizada de emergencia, es nuevo método para procesar muestras de saliva cuando se realizan pruebas de infección por covid-19 de una manera más rápida y menos complicada.
LEA: OMS pide a países que se unan a su mecanismo para garantizar acceso a una vacuna
“La prueba SalivaDirect para la detección rápida de SARS-CoV-2 es otro factor de cambio en la innovación de pruebas que reducirá la demanda de recursos de pruebas escasos”, dijo el subsecretario de Salud y Coordinador de Pruebas de covid-19, Almirante Brett P.
Por otra parte, el comisionado de la FDA, Stephen M. Hahn, recalcó que 'proporcionar este tipo de flexibilidad para procesar muestras de saliva para detectar la infección por covid-19 es innovador en términos de eficiencia y evita la escasez de prueba cruciales como los reactivos”.
ADEMÁS: Rusia ya produjo el primer lote de vacunas contra el covid-19
¿Cómo funciona?
De acuerdo con la FDA, el SalivaDirect no requiere ningún tipo especial de hisopo o dispositivo de recolección, pues se puede hacer la prueba con cualquier recipiente estéril.De igual manera, no requiere un paso de extracción de ácido nuleico por separado, haciendo más eficiente la cantidad de diagnósticos a realizar.
'La metodología SalivaDirect ha sido validada y autorizada para su uso con diferentes combinaciones de reactivos e instrumentos de uso común, lo que significa que la prueba podría usarse ampliamente en la mayoría de los laboratorios de alta complejidad', explica la FDA.
TAMBIÉN: Latinoamérica podría tener la vacuna contra el coronavirus antes de lo previsto